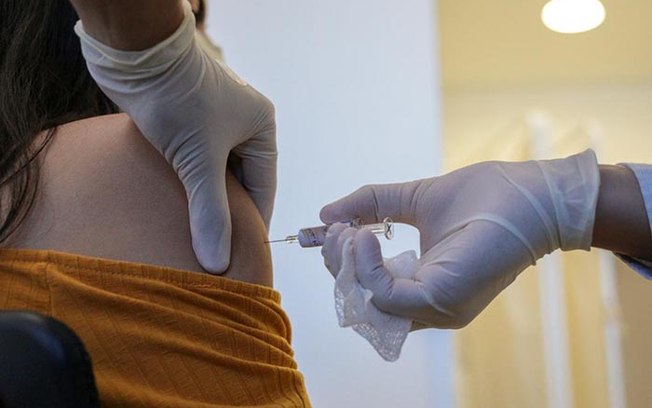
Nesta terça-feira (10), o laboratório chinês Sinovac Biotech se manifestou após a Anvisa paralisar os testes da CoronaVac comandados pelo Butantan no Brasil devido a morte de um voluntário . Em nota, a empresa garantiu a segurança do imunizante e ressaltou que o “evento adverso grave” não tem a ver com a vacina.
Na segunda-feira (9), a autoridade sanitária do Brasil anunciou que suspendeu os ensaios clínicos da vacina Coronavac “após a ocorrência de um evento adverso grave”, em 29 de outubro, com um voluntário. A Agência Nacional de Vigilância Sanitária (Anvisa) não forneceu detalhes sobre o incidente, referindo apenas que a categoria de “evento adverso” pode incluir a morte, efeitos secundários potencialmente fatais, incapacidade ou invalidez persistente ou significativa, hospitalização ou outro “evento clinicamente significativo”.
“Com a interrupção do estudo, nenhum novo voluntário poderá ser vacinado”, precisou a agência, acrescentando que vai “avaliar os dados observados até o momento e julgar o risco/benefício da continuidade” dos testes.
O órgão público que coordena os testes de vacinas no Brasil, o Instituto Butantan, disse que ficou “surpreendido” com a decisão e dará uma conferência de imprensa às 14:00 (GMT) (mesma hora em Lisboa) de hoje.
A suspensão dos ensaios clínicos da Coronavac, que envolve nove mil voluntários, ocorreu um dia depois de o gigante farmacêutico norte-americano Pfizer anunciar que a sua vacina contra a covid-19 alcançou 90% de eficácia nos teste e no mesmo dia no início das obras da nova fábrica do Instituto Butantan, que produzirá a vacina no Brasil após aprovação.
As vacinas candidatas da Pfizer e do Sinovac estão em ensaios da Fase 3, a última fase antes de receberem aprovação regulamentar. Ambas estão a ser testadas no Brasil, o segundo país mais afetado pela pandemia, com mais de 162.000 mortes.